Lancet:乌司奴单抗
来源: 最后更新:22-12-06 12:44:28
-
克罗恩病是一种原因不明的肠道炎症性疾病,在胃肠道的任何部位均可发生,但多发于末端回肠和右半结肠,临床表现为腹痛、腹泻、肠梗阻,伴有发热、营养障碍等肠外表现。病程多迁延,反复发作,不易根治。目前尚无根治的一般方法,许多病人出现并发症时,需进行手术治疗。
阿达木单抗注射液是全球首个获批上市的全人源抗肿瘤坏死因子ɑ(TNF-ɑ)单克隆抗体,能特异性地与可溶性人TNF-ɑ结合并阻断其与细胞表面TNF受体p55和p75的相互作用,从而有效地阻断TNF-ɑ的致炎作用。
乌司奴单抗是一种全人源单克隆抗体,可特异性结合白细胞介素IL-12和IL-23的p40蛋白亚单位,亲和力高。IL-12和IL-23是天然产生的细胞因子,在人体的急性和慢性炎症均发挥重要作用。

SEAVUE研究是一项全球多中心RCT研究,旨在未使用过生物制剂治疗(bio-na?ve) 的中重度活动性CD患者中,比较乌司奴单抗(UST)和阿达木单抗(ADA)治疗1年的疗效和安全性。
多中心、双盲SEAVUE试验涉及386名皮质类固醇或免疫调节剂治疗无效的生物制剂初治克罗恩病患者。所有患者的克罗恩病活动指数(CDAI)评分在220到450之间,并且在回结肠镜检查时,至少检测到一处溃疡。参与者按1:1的比例随机接受皮下注射阿达木单抗(无枸橼酸盐;基线时160mg,第2周70mg,然后每2周40mg)或乌司奴单抗(首先静脉注射6mg/kg,然后每8周皮下注射90mg)。

主要终点是第52周时的临床缓解,定义为CDAI得分小于150。主要次要终点包括临床反应、无皮质类固醇缓解、内镜缓解、患者报告的CDAI成分缓解和第16周时的临床缓解。所有终点的结果在统计学上相似,乌司奴单抗组和阿达木单抗组1年时的临床缓解率分别为64.9%和61.0%(组间差异 4%,95% CI –6 至 14;P=0.417)。不过,乌司奴单抗组191 名患者中的 29 名(15%)和阿达木单抗组 195 名患者中的 46 名(24%)在第 52 周之前停止了研究治疗。
这两种治疗都显示出快速起效和良好的内窥镜检查结果;两组内镜缓解率相当,乌司奴单抗组和阿达木单抗组分别为28.5%和30.7%(P=0.631)。

在次要终点中,乌司奴单抗表现出一定的优越性,在第16周有反应的患者中,52周时的临床反应维持得更好(88.6%对78.0%;P=0.016),从基线检查前7天到第52周,液体/软性大便减少更多(–19.9 对–16.2;P=0.004),并且从基线检查前7天到第52周,液体/软性大便总数和腹痛得分减少更多(–29.6 对–25.1;P=0.013)。
两组的安全性与之前的报告一致。 乌司奴单抗组 191 名患者中有 4 名(2%)报告了严重感染,阿达木单抗组 195 名患者中有 5 名(3%)报告了严重感染。 在研究的第 52 周内没有发生死亡。
原始出处:
Sands BE, Irving PM, Hoops T, Izanec JL, Gao LL, Gasink C, Greenspan A, Allez M, Danese S, Hanauer SB, Jairath V, Kuehbacher T, Lewis JD, Loftus EV Jr, Mihaly E, Panaccione R, Scherl E, Shchukina OB, Sandborn WJ; SEAVUE Study Group.Ustekinumab versus adalimumab for induction and maintenance therapy in biologic-naive patients with moderately to severely active Crohn's disease: a multicentre, randomised, double-blind, parallel-group, phase 3b trial.Lancet. 2022 Jun 11;399(10342):2200-2211. doi: 10.1016/S0140-6736(22)00688-2
以上内容仅授权39健康网独家使用,未经版权方授权请勿转载。此文出于传递更多信息之目的,并不意味着赞同其观点或证实其描述。文章内容仅供参考,具体治疗及选购请咨询医生或相关专业人士。
免责声明:本文系转载,版权归原作者所有;旨在传递信息,其原创性以及文中陈述文字和内容未经本站证实。
帮同学化妆最高日入近千 帮朋友化妆帮同学化妆最高日入近千?浙江大二女生冲上热搜,彩妆,妆容,模特,王
2023吉林省紧缺急需职业工种目录政策解读 2024张杰上海演唱会启东直通车专线时间+票价 马龙谢幕,孙颖莎显示统治力,林诗栋紧追王楚钦,国乒新奥运周期竞争已启动 全世界都被吓了一跳(惊吓全世界)热门标签
热门文章
-
帮同学化妆最高日入近千 帮朋友化妆 24-10-07
-
2024杭甬运河宁波段恢复全线通航 杭甬运河属于几级航道 24-10-07
-
2024宁波羽毛球亚锦赛有哪些选手参加(宁波市羽毛球锦标赛) 24-10-07
-
通过对华电车征税提议 通过对华电车征税提议的建议 24-10-07
-
关于网传“男子接亲被加要18万彩礼”情况说明 24-10-07
-
释新闻|登上热搜的哀牢山在哪里,山里都有什么? 24-10-07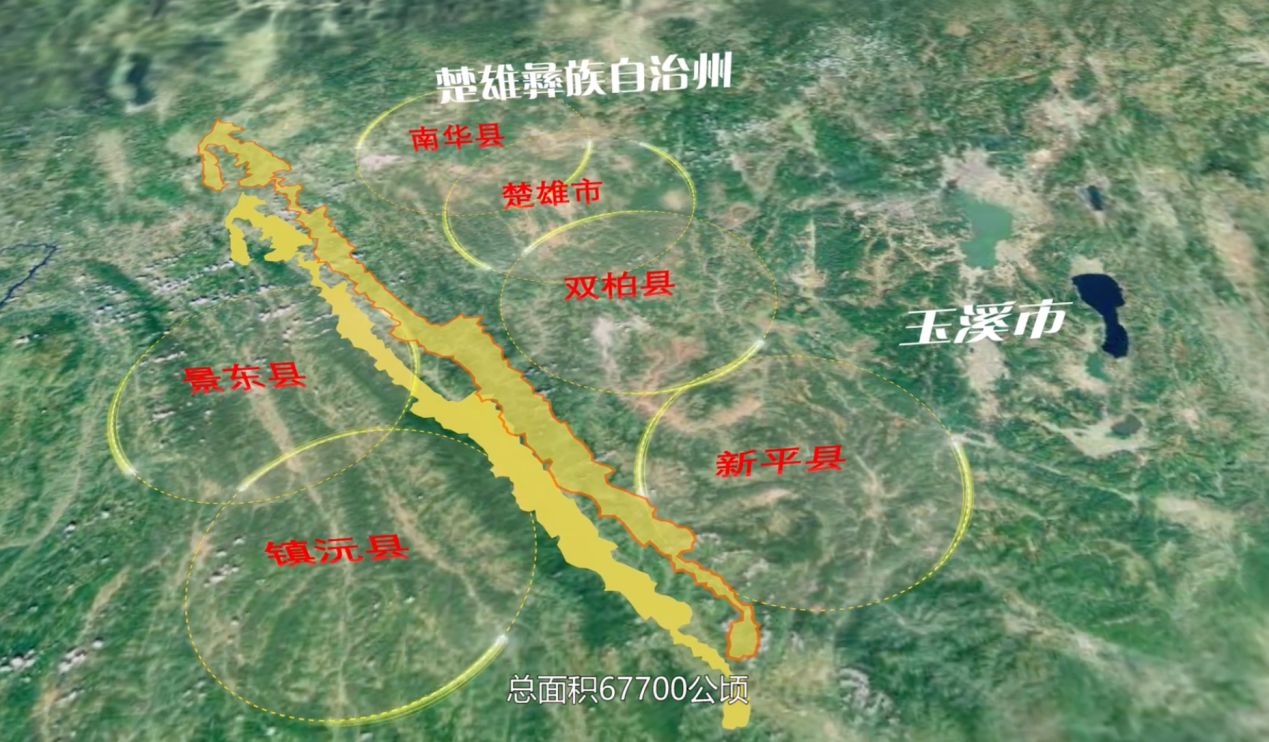
-
2024年江门市公墓清明节祭扫预约方式汇总 24-10-07
-
襄阳市图书馆10月活动(襄阳市图书馆国庆开放时间) 24-10-06
-
2023青岛凤凰音乐节官方有哪些售票平台? 24-10-06
-
民宿老板回应哀牢山爆火:国庆期间房源天天爆满,平时约90元一晚涨到约240元 24-10-06